Qual é o valor da energia de ativação?
Índice
- Qual é o valor da energia de ativação?
- Como descobrir energia de ativação?
- Como achar a energia de ativação no gráfico?
- O que altera a energia de ativação?
- O que vem a ser energia de ativação?
- Qual a unidade de energia de ativação?
- Quais fatores influenciam na velocidade da energia de ativação?
- Qual o valor da energia de ativação?
- Como calcular a energia de ativação de uma reação?
- Como calcular a energia de ativação através de um gráfico?
- Como analisar a energia de ativação?
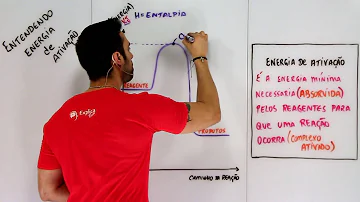
Qual é o valor da energia de ativação?
Além disso, a energia de ativação é dada pela diferença entre a energia necessária para a reação iniciar e formar o complexo ativado (topo mais alto) e a energia que os reagentes já possuíam no início da reação.
Como descobrir energia de ativação?
Química
- Dessa forma, podemos concluir que a energia de ativação (Eat) é a diferença entre a energia necessária para que a reação tenha início (E) e a energia própria contida nos reagentes (Epr):
- A energia de ativação é um obstáculo para que a reação ocorra e ela é necessária para romper as ligações dos reagentes.
Como achar a energia de ativação no gráfico?
No gráfico percebemos que a energia de ativação é o caminho dos reagentes até o ponto mais energético (mais alto) do gráfico que é o complexo ativado, momento reacional onde reagentes e produtos coexistem. Após isso está representada a formação dos produtos.
O que altera a energia de ativação?
O que é energia de ativação? Energia mínima necessária para formar o complexo ativado em uma reação química, ela pode ser diminuída com a ação de catalisadores. ... Porém, o tempo para formar o complexo ativado indica se uma reação química será mais rápida ou mais lenta que a outra.
O que vem a ser energia de ativação?
De uma forma bem objetiva, podemos definir a energia de ativação (Eat) como a energia necessária para a ocorrência de uma reação. Por exemplo, para que a chama do fogão seja formada, é necessário fornecer uma faísca elétrica para permitir a ocorrência da reação entre o gás oxigênio e o gás de cozinha.
Qual a unidade de energia de ativação?
Tipicamente a energia de ativação é considerada como sendo a energia em quilojoule necessária para que 1 mol de reagente reaja.
Quais fatores influenciam na velocidade da energia de ativação?
Alguns fatores que podem influenciar a velocidade de uma reação são: a temperatura, a pressão, a concentração, a superfície de contato e por fim, o catalisador e o inibidor.
Qual o valor da energia de ativação?
Como pode ser visto, a inclinação resultante desse cálculo é igual ao valor de –Ea / R. Isso implica que, se desejar obter o valor da energia de ativação por meio dessa expressão, uma simples limpeza deve ser realizada, resultando em: Aqui, o valor de m e R é conhecido como uma constante igual a 8.314 J / K · mol.
Como calcular a energia de ativação de uma reação?
Outra maneira de calcular a energia de ativação de uma reação é representar graficamente ln k (a constante de taxa) versus 1 / T (o inverso da temperatura em Kelvin). O gráfico formará uma linha reta expressa pela equação:
Como calcular a energia de ativação através de um gráfico?
Para calcular a energia de ativação através da construção de um gráfico, de acordo com a equação de Arrhenius, é necessário que as constantes de taxa para a reação de decomposição do acetaldeído tenham sido medidas em cinco temperaturas diferentes e se deseja determinar a energia de ativação para a reação, que é expressa como:
Como analisar a energia de ativação?
A forma mais comum de analisar a energia de ativação e o complexo ativado é utilizando um gráfico, o qual apresenta, como padrão, energia ou entalpia (em KJ ou Kcal) no eixo y, o caminho da reação (do reagente em direção aos produtos) no eixo x, e uma curva, como podemos ver a seguir:














