Pode-se afirmar que nas CNTP 3 Mols de gás nitrogênio ocupam qual volume em litros?
Pode-se afirmar que nas CNTP 3 Mols de gás nitrogênio ocupam qual volume em litros?
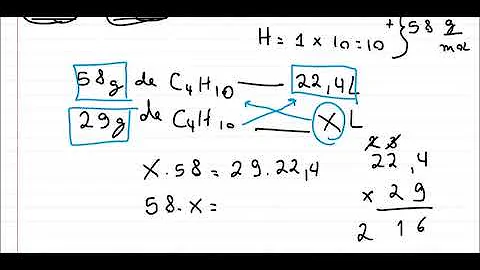
O volume molar corresponde ao volume ocupado por qualquer gás nas CNTP, que é igual a 22,4 L.
Como calcular o volume de um mol de gás na CNTP?
Sabendo que o volume de 1 mol de gás na CNTP é 22,4 L, basta multiplicar por 2 para saber o volume de 2 mol. Temos então a resposta, 2 . 22,4 = 44,8 L – letra “d”. 2. Calcule o volume de uma amostra de 3,4 mol de gás hidrogênio (H 2) na CNTP.
Qual é o volume de um gás?
V é o volume que um gás ocupa e corresponde ao volume do recipiente no qual se encontra. As unidades de volume estão relacionadas a seguir: 1 L = 10 - cm³ = mL
Qual a pressão normal dos gases?
A pressãonormal equivale a 1 atm, que é igual a 760 mmHg, que é aproximadamente igual a 100 kPa. A temperaturanormal equivale a 0°C, que é igual a 273 K. Aplicando esses valores de CNTP na equação de estado dos gases, pode-se calcular o volume molar e a constante dos gases (R).
Qual o volume molar de um gás?
Sabendo-se que o volume molar de um gás nas condições normais de temperatura e pressão (CNTP) é igual a 22,4 L e que R = 0,082 atm ∙ L ∙ K –1 ∙ mol –1, o maior número de moléculas está contido em 1,0 L de:














