Qual a interferência da energia de ativação na velocidade das reações?
Índice
- Qual a interferência da energia de ativação na velocidade das reações?
- O que é energia de ativação de uma reação?
- Quanto mais alta a energia de ativação mais lenta será a reação?
- Qual o valor da energia de ativação da reação?
- O que é um catalisador e como ele influencia na velocidade das reações?
- O que é energia de ativação Qual a relação entre uma enzima e a energia de ativação de uma reação?
- Qual é o efeito do catalisador sobre a energia de ativação?
- O que é energia de ativação quando ela é aumentada ou diminuída O que acontece com a velocidade da reação química?
- Porque a energia de ativação indica se a reação é lenta ou rápida?
- Qual a energia de ativação para uma reação?
- Como influencia a velocidade de uma reação?
- Qual a influência da temperatura sobre a velocidade das reações?
- Qual a energia necessária para a ocorrência de uma reação?
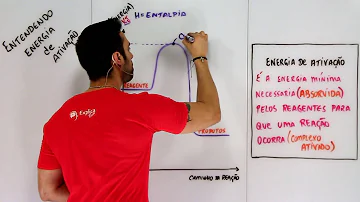
Qual a interferência da energia de ativação na velocidade das reações?
Assim, quanto maior a energia de ativação, mais difícil será para que a reação ocorra e, consequentemente, ela se dará de forma mais lenta. O contrário também é verdadeiro, reações com uma menor energia de ativação ocorrem com maior velocidade.
O que é energia de ativação de uma reação?
De uma forma bem objetiva, podemos definir a energia de ativação (Eat) como a energia necessária para a ocorrência de uma reação. Por exemplo, para que a chama do fogão seja formada, é necessário fornecer uma faísca elétrica para permitir a ocorrência da reação entre o gás oxigênio e o gás de cozinha.
Quanto mais alta a energia de ativação mais lenta será a reação?
Especificamente, quanto maior for a energia de ativação, mais lenta será a reação química. Isso acontece porque as moléculas só podem completar a reação depois de atingirem o topo da barreira da energia de ativação.
Qual o valor da energia de ativação da reação?
Além disso, a energia de ativação é dada pela diferença entre a energia necessária para a reação iniciar e formar o complexo ativado (topo mais alto) e a energia que os reagentes já possuíam no início da reação.
O que é um catalisador e como ele influencia na velocidade das reações?
Um catalisador é uma substância que aumenta a velocidade de uma reação química sem estar sendo consumido por ela. O catalisador não tem efeito sobre o equilíbrio de uma reação, ele pode acelerar ou retardar a velocidade na qual uma reação atinge o equilíbrio, mas ele não afeta a composição no equilíbrio.
O que é energia de ativação Qual a relação entre uma enzima e a energia de ativação de uma reação?
a enzima provoca uma diminuição da energia de ativação necessária para que uma reação química aconteça e isso facilita a ocorrência da reação. Na catálise de uma reação química, as enzimas interagem com os substratos, formando com eles, temporariamente, o chamado complexo enzima-substrato.
Qual é o efeito do catalisador sobre a energia de ativação?
Em geral, o catalisador acelera a reação encontrando um caminho alternativo (um atalho), que em química traduz-se como um mecanismo de reação diferente, entre reagentes e produtos. ... Esse novo caminho tem uma energia de ativação menor que a do caminho original.
O que é energia de ativação quando ela é aumentada ou diminuída O que acontece com a velocidade da reação química?
Energia de ativação é a energia mínima para que uma reação química possa ocorrer, ou seja, é um dos fatores determinantes para a ocorrência de uma reação, juntamente com o contato e a colisão favorável entre as moléculas dos reagentes.
Porque a energia de ativação indica se a reação é lenta ou rápida?
Energia de ativação é a energia necessária para que uma reação ocorra. ... Se a energia de ativação for menor, consequentemente a energia absorvida será menor e será absorvida em um menor tempo; consequentemente a reação ocorrerá mais rapidamente.
Qual a energia de ativação para uma reação?
Energia de ativação é a energia mínima para que uma reação química possa ocorrer, ou seja, é um dos fatores determinantes para a ocorrência de uma reação, juntamente com o contato e a colisão favorável entre as moléculas dos reagentes. Modelo de colisão favorável entre os reagentes de uma reação
Como influencia a velocidade de uma reação?
Temos alguns fatores que podem influenciar a velocidade de uma reação conforme já citamos e são eles: a temperatura, a pressão, a concentração, a superfície de contato e por fim, o catalisador e o inibidor.
Qual a influência da temperatura sobre a velocidade das reações?
Isso faz com que haja mais moléculas com energia suficiente para reagir, o que acarreta no aumento da velocidade da reação. O primeiro cientista que estudou essa influência da temperatura sobre a velocidade das reações foi Jacobus Vant’t Hoff, no final do século XIX.
Qual a energia necessária para a ocorrência de uma reação?
Segundo a Termoquímica, durante a ocorrência de uma reação, cada reagente apresenta certa quantidade de energia e, além dessa, ele também deve entrar em contato com uma energia proveniente do meio externo. De uma forma bem objetiva, podemos definir a energia de ativação (Eat) como a energia necessária para a ocorrência de uma reação.














