Qual a utilidade do indicador de pH?
Índice
- Qual a utilidade do indicador de pH?
- Como agem os indicadores ácido-base?
- Quais os indicadores de ácido e base?
- Quais os tipos de indicadores naturais de ácidos e base?
- O que são e como agem os indicadores Ácido-base?
- Porque a fenolftaleína fica incolor?
- Qual é o papel da fenolftaleína?
- ¿Cómo funciona un indicador de pH?
- ¿Qué es un parámetro de pH?
- ¿Qué es una indicación aproximada del pH?
- ¿Qué son los medidores de pH?
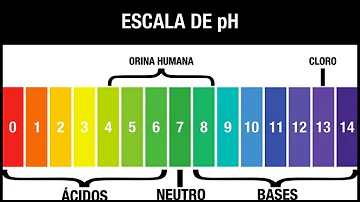
Qual a utilidade do indicador de pH?
Um indicador de pH, também chamado indicador ácido-base, é um composto químico que é adicionado em pequenas quantidades a uma solução, permitindo conhecer se seu pH se encontra acima ou abaixo de uma determinada faixa de valores que varia conforme o indicador escolhido.
Como agem os indicadores ácido-base?
Os indicadores ácido-base são substâncias naturais e sintéticas que mudam de cor de acordo com o pH do meio. Os indicadores ácido-base são substâncias naturais ou sintéticas que possuem a capacidade de mudar de cor de acordo com o pH do meio.
Quais os indicadores de ácido e base?
São exemplos de indicadores ácido-base: fenolftaleína, alaranjado de metila, papel tornassol, azul de bromotimol. Alguns indicadores naturais também podem ser utilizados, como o repolho roxo e a flor hortência e o hibisco.
Quais os tipos de indicadores naturais de ácidos e base?
Indicadores ácido-base naturais
- As substâncias presentes no extrato de repolho roxo que o fazem mudar de cor em ácidos e bases são as antocianinas. ...
- O tronco e as folhas de certas nogueiras também possuem outro tipo de substância que serve como indicador ácido-base natural, que é a esculina.
O que são e como agem os indicadores Ácido-base?
Os indicadores ácido-base são substâncias que, por suas propriedades físico-químicas, apresentam a capacidade de mudar de cor na presença de um ácido ou de uma base. Os indicadores ácido-base são substâncias naturais ou sintéticas que têm a propriedade de mudarem de cor em função do pH do meio.
Porque a fenolftaleína fica incolor?
Exemplo: se adicionarmos na solução de fenolftaleína um ácido ela se torna incolor, pois, o aumento da concentração de H+ desloca o equilíbrio.
Qual é o papel da fenolftaleína?
A fenolftaleína é um exemplo de indicador ácido-base sintético muito usado em laboratório. Ela fica incolor em meio ácido e adquire uma coloração rosa intensa (como mostra a imagem inicial) em meio básico. O princípio de funcionamento da fenolftaleína pode ser visto no texto Indicadores de pH.
¿Cómo funciona un indicador de pH?
En la actualidad los indicadores de pH tienen una gran variedad de aplicaciones, desde las farmacéuticas, donde se aplica colorante de teñido al cinco por ciento; la industria alimentaria y hasta la petrolera, donde es determinante de la alcalinidad del fango procedente de los pozos. ¿Cómo funciona un indicador?
¿Qué es un parámetro de pH?
Este parámetro se expresa de la siguiente manera con la ecuación de Henderson-Hasselbalch: pH = pKa + log10 ( [A–]/ [HA]). En la expresión anterior, el pKa representa el logaritmo negativo de la constante de disociación de ácidos, y las concentraciones molares [A–] y [HA] son las del ácido débil y su base conjugada, respectivamente.
¿Qué es una indicación aproximada del pH?
Medición de pH Una indicación aproximada del pH puede ser obtenida usando indicadores o cintas de pH, que cambian de color en función de la variación del nivel de pH. Esos indicadores presentan limitaciones en términos de exactitud y pueden ser difíciles de interpretar correctamente en muestras oscuras o coloridas.
¿Qué son los medidores de pH?
Estos medidores de pH ofrecen total funcionalidad en un tamaño portátil para uso en laboratorio o en el campo. Entre los recursos disponibles, están incluidos salida RS232, fijación de lectura de datos, selección de ºC o ºF, desconexión automática, indicación de sobrecarga y compensación manual o automática de temperatura y otros más.














