Como calcular o volume ocupado?
Como calcular o volume ocupado?
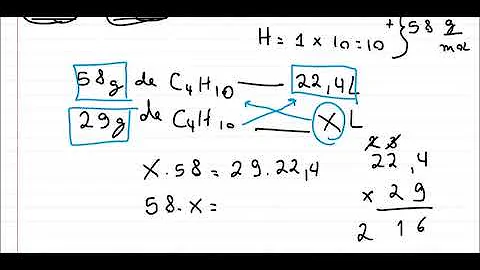
Assim, quando consideramos as Condições Normais de Temperatura e Pressão (CNTP), em que a pressão é igual a 1 atm e a temperatura é de 273 K (0ºC), temos que o volume ocupado por 1 mol de qualquer gás sempre será de 22,4 L. Esse valor corresponde ao volume molar dos gases.
Como calcular o volume em estequiometria?
Cálculo de volumes
- Escrever a equação: N2 (g) + H2 (g) → NH3 (g)
- Balancear: 1 N2 (g) + 3 H2 (g) → 2 NH3 (g)
- Relacionar: 1 mol N2 ocupa 22,4 L (CNTP). 1 mol NH3 = 17 g → 2 mols NH3 = 2 · 17 = 34 g. 1 N2(g) + 3 H2(g) → 2 NH3(g) 1 mol N2 2 mols NH3 22,4 L ,4 L m.
- Usar a regra de três para resolver o problema.
Como calcular o volume de um composto químico?
Volume da solução mL ou 0,1 L (depois de dividir por 1000) Massa do soluto na solução 1 = 10 g. Volume da solução mL ou 0,1 L (depois de dividir por 1000)...Os dados fornecidos pelo exercício foram:
- Volume da solução mL.
- Concentração em mol/L da solução 1 = 3. ...
- Volume da solução mL.
Como calcular o volume de um mol de gás na CNTP?
Sabendo que o volume de 1 mol de gás na CNTP é 22,4 L, basta multiplicar por 2 para saber o volume de 2 mol. Temos então a resposta, 2 . 22,4 = 44,8 L – letra “d”. 2. Calcule o volume de uma amostra de 3,4 mol de gás hidrogênio (H 2) na CNTP.
Qual a pressão normal da IUPAC?
Veja que há até uma discrepância nos textos da Sociedade Brasileira de Química. A IUPAC define pressão normal como 101 325 Pa (1 atm) até hoje, embora ela não recomende usar. Para mim, o volume molar nas CNTP é 22,4 L/mol e o volume molar nas CPTP é 22,7 L/mol. Acho pertinente esta discussão.
Qual é o volume em exercícios?
Em exercícios, é muito comum considerarmos o volume nas condições normais de temperatura e pressão (CNTP), que equivale a 22,4 L, por isso é importante conhecer esse valor. 1. (PUC Minas) Sob condições apropriadas, gás acetileno (C 2 H 2 (g)) e ácido clorídrico reagem para formar cloreto de vinila, C 2 H 3 Cl (g).














